Products
효과적이고 안정적인믿을 수 있는 의약품
- 상세 정보
- 사용상 주의사항
- 성분함량
-
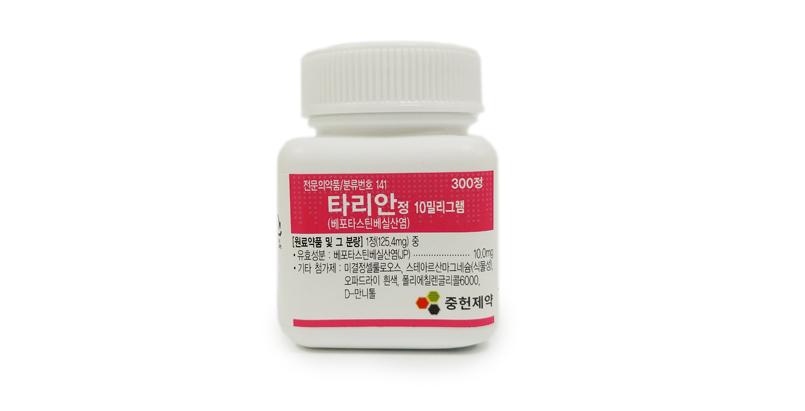
1정(125.4mg) 중
유효 성분 : 베포타스틴베실산염(JP) 10.0mg
첨가제 : D-만니톨, 미결정셀룰로오스, 폴리에칠렌글리콜6000, 스테아르산마그네슘, 오파드라이 흰색 (03B28796)
- 성상
- 흰색의 원형 필름코팅정
- 효능/효과
- 다년성 알레르기성 비염, 만성 두드러기, 피부질환에 수반된 소양증(습진, 피부염, 피부소양증, 양진)
- 용법/용량
- 통상, 성인에게는 베실산 베포타스틴으로서 1회 10mg을 1일 2회 경구 투여한다.
또한 연령, 증상에 따라 적절하게 증감한다.
- 저장방법
- 기밀용기, 실온보관(1~30℃)
- 유효기간
- 제조일로부터 36개월
-
1. 다음 환자(경우)에는 투여하지 말 것.
- 이 약 성분에 과민증이 있는 환자
-
2. 다음 환자에는 신중히 투여할 것.
- 1) 신기능장애가 있는 환자
- 2) 간기능장애가 있는 환자
- 3) 고령인 환자
-
3. 이상반응
- 임상시험에서 총 증례 1,446명 중, 부작용이 137명(9.5%) 보고되었다
- 1) 정신신경계 : 졸음, 권태감, 두통, 두중감, 현기증
- 2) 소화기계 : 구갈, 구내건조, 설염, 오심, 구토, 위통, 위부불쾌감, 설사
- 3) 혈액계 : 백혈구수 변동, 호산구과다증
- 4) 간장 : AST(GOT), ALT(GPT), r-GTP, LDH, 총빌리루빈 상승
- 5) 신장 : 뇨단백, 뇨당, 뇨잠혈, 뇨우로빌리노겐
- 6) 피부 : 발진, 종창의 과민반응
국내 시판 후 조사 결과(정제)
국내에서 재심사를 위하여 6년 동안 3,717명의 환자를 대상으로 실시한 시판 후 조사 결과 유해사례 발현율은 인과관계와 상관없이 1.8%(68명/3,717명, 80건)로 보고되었다. 졸음 1.26%(47명/3,717명, 47건), 갈증 0.30%(11명/3,717명, 11건), 복부불쾌 0.27%(10명/3,717명, 10건), 권태 0.11%(4명/3,717명, 4건), 얼굴부종 0.05%(2명/3,717명, 2건), SGOT 상승, SGPT 상승, 두통, 두근거림, 얼굴홍조, 쓴맛 각 0.03%(1명/3,717명, 1건)순으로 조사되었다. 이 약과 인과관계를 배제할 수 없는 유해사례인 약물유해반응 발현율은 1.4%(52명/3,717명, 62건)로 보고되었다. 졸음 1.13%(42명/3,717명, 42건), 갈증 0.24%(9명/3,717명, 9건), 복부불쾌 0.11%(4명/3,717명, 4건), 권태 0.08%(3명/3,717명, 3건), 얼굴홍조, SGOT 상승, SGPT 상승 각각 0.03%(1명/3,717명, 1건)이었다. 국내 시판 후 조사기간 동안 발생한 예상하지 못한 유해사례의 발현율은 인과관계와 상관없이 0.13%(5명/3,717명, 5건)이었으며, 얼굴부종 0.05%(2명/3,717명, 2건), 두근거림, 얼굴홍조, 쓴맛 각각 0.03%(1명/3,717명, 1건)로 보고되었다. 이 중 이 약과 인과관계를 배제할 수 없는 유해사례인 약물유해반응으로 얼굴홍조 1건이 보고되었다. 국내 시판 후 조사기간 동안 발생한 중대한 유해사례는 보고되지 않았다. - ◇ 보다 자세한 사항은 제품 상세정보에서 참조한다.
- ◇ 개정된 사항은 식품의약품안전처 온라인 의약도서관(http://drug.mfds.go.kr/html/index.jsp)을 참고한다.